2024年10月01日
我が国独自のナノ粒子性薬剤送達システムを用いた次世代ワクチンの新型コロナ ウイルスに対する優れたキラーT細胞誘導と感染防御性能を動物モデルで実証 ― 将来の感染症ワクチン開発への幅広い応用の可能性 ―
発表のポイント
◆プルランナノゲル(略称PNG)は多糖プルランを主成分とする我が国独自の免疫系指向性・ナノ粒子性の薬剤送達システムです。今回、PNGを応用した新型コロナウイルスに対する新規ワクチン(以下PNGワクチン)を新たに創製しました。
◆ PNGワクチンがウイルスに対する優れた感染防御効果を示すことを動物モデルで確認しました。この効果はPNGワクチンが、リンパ節内の抗原提示細胞への受容体依存的なワクチン送達を通じて、ウイルス感染に有効に対応できる良質なキラーT細胞を体内に誘導するという働きに依ることも明らかにしました。
◆PNGワクチン技術は今後、様々な感染症に対し幅広く応用できると期待されます。
概 要
長崎大学大学院医歯薬学総合研究科 腫瘍医学分野の池田 裕明 教授、東京大学大学院医学系研究科 国際保健学専攻 国際生物医科学講座のMOI MENG LING教授、京都大学大学院医学研究科 免疫細胞生物学の秋吉 一成特任教授、愛知県がんセンター(研究所) 腫瘍免疫制御TR分野の村岡 大輔 ユニット長、ユナイテッド・イミュニティ株式会社の原田 直純 代表取締役会長らによる研究グループは、今回、新型コロナウイルスに対する次世代ワクチンを新たに創製しました。本ワクチンは秋吉教授が発明した多糖ナノ粒子「プルランナノゲル(以下PNG)」を免疫系指向性の薬剤送達システムとして採用し、新型コロナウイルスのスパイク蛋白の断片をワクチン抗原としています。
マウスを用いた新型コロナウイルスの感染試験では、PNGワクチンの事前投与により体内のウイルス量が有意に低下し、ウイルス感染に対して全例が生存しました。これに対しPNGを用いないワクチンでは、3割近くのマウスがウイルス感染で死亡しました。PNGワクチンの優れた感染防御効果は、PNGがリンパ節内の重要な抗原提示細胞であるマクロファージに受容体依存的にワクチン抗原を送達してキラーT細胞に対する抗原提示を促進することで、ウイルス感染に有効に対応できる良質なキラーT細胞を特に誘導するという作用機序に依ります。
以上の成果は、リンパ節内のマクロファージへのワクチン送達により良質なキラーT細胞を積極的に誘導するという新しいワクチン戦略の可能性を示し、またPNGがこれを実現する理想的な薬剤送達システムであることを示しています。我が国独自の本技術は今後、他の病原性ウイルス、特に将来のパンデミックに対する次世代ワクチン技術として応用展開されると期待されます。本技術のmRNAワクチンへの応用研究も鋭意推進されています。
この研究は国立研究開発法人日本医療研究開発機構(AMED)ワクチン開発のための世界トップレベル研究開発拠点の形成事業およびワクチン・新規モダリティ研究開発事業の支援を得て行われました。本成果はワクチン学に関する国際学術専門誌「npj Vaccines」に2024年9月18日付で掲載されました。
発表内容
《研究背景》
新型コロナウイルス(SARS-CoV-2又はCOVID-19ウイルス)を始めとする病原性ウイルスに対するワクチンの開発では、対象とするウイルスの全ての変異株に対して長期的に防御できる免疫応答を誘導できるか否かが重要になっています。ワクチン接種又は新型コロナウイルスの感染により、同ウイルスに対する中和抗体及びT細胞が体内に誘導され、これら免疫系の働きによって同ウイルスのさらなる感染が抑制されます。中和抗体はウイルス表面の蛋白(新型コロナウイルスではスパイク蛋白)に結合することでウイルスの細胞への感染を阻害します。しかし中和抗体が標的とする蛋白に生じる突然変異によって、中和抗体の感染阻害活性が減弱することが知られています。また、中和抗体の持続性には限界があることも分かっています。一方、T細胞はウイルスに感染した細胞を排除することで体内での感染の進行を抑止します。特に重要な特徴として、T細胞がウイルス感染細胞を排除する際に認識する部位は、ウイルスの突然変異の影響を比較的受けにくいことが分かっています。またT細胞は防御免疫の長期持続性(免疫記憶)にも寄与します。よって、幅広いウイルス変異株に長期的に有効なワクチンの開発において、中和抗体に加えてT細胞活性化の重要性が高まっています。
《研究内容》
プルランナノゲル(以下PNG。注1)は、多糖プルランから成る100ナノメートル以下の球状ナノ粒子です(図1)。多糖プルランは食品、化粧品、医薬品の添加物として幅広く利用されている身近な多糖です。PNGの内部は多糖プルランが構成するネットワーク構造(ハイドロゲル構造)となっており、その間隙に蛋白、ペプチド、低分子化合物、オリゴ核酸等の様々な成分を搭載することができます。これまでPNGは、がん治療用ワクチンの薬剤送達システムとして長年にわたり臨床応用が試みられてきました。またPNGを用いることで、皮下投与されたワクチンがリンパ節に速やかに移行し、マクロファージ(注2)や樹状細胞といったプロフェッショナルな抗原提示細胞に効率よく取り込まれてT細胞への抗原刺激を促進することも過去に明らかにしています(Muraoka et al., ACS Nano 2014)。
本研究では、PNGに新型コロナウイルスのスパイク蛋白の断片をワクチン抗原として搭載した新型コロナウイルスワクチンを新たに創製し(図1)、ウイルス感染に対する防御効果を新型コロナウイルスのマウス感染モデルで初めて検討しました。PNGワクチンを事前に皮下投与したマウスでは、ウイルス感染後の生存率が100%となり、感染に伴う体重減少も見られませんでした(図2)。PNGワクチンは唾液や肺等の臓器におけるウイルス量の有意な低下ももたらしました。一方でPNGを用いないワクチンでは、ウイルス感染後の生存率は約7割に留まり、感染による体重減少も認められました。ワクチンを全く投与しないマウスでは生存率は0%でした。
PNGワクチンの優れた感染防御効果を支えるメカニズムを明らかにするために、PNGワクチンを投与したマウスにおける新型コロナウイルスに特異的なCD8陽性キラーT細胞(注3)の変化を調べました。その結果、PNGワクチンを投与したときは、PNGを用いないワクチンと比較して、新型コロナウイルス感染細胞を認識できるCD8陽性キラーT細胞が脾臓と肺で顕著に増加していました(図3)。誘導されたCD8陽性キラーT細胞のクローン毎の違いをT細胞受容体(略称TCR。注4)のレパトア解析を用いて詳しく調べました。まずPNGワクチン投与直後は、異なるTCRを有する様々な存在頻度のCD8陽性キラーT細胞クローンが増加しました。その後のウイルス感染時は、その中の一部のCD8陽性キラーT細胞クローンがウイルスに反応し増殖しました。この一部のCD8陽性T細胞クローンはPNGワクチンで誘導された後、ウイルス感染に反応して迅速に増殖拡大し、ウイルス感染細胞の排除の中心を担っていると考えられます。ただし、これらの有用なCD8陽性T細胞クローンの存在頻度は、PNGワクチン投与直後はごく低いものでした。つまり、ワクチン投与直後に存在頻度が低かったCD8陽性T細胞クローンがウイルス感染時に比較的高頻度になり、一方でワクチン投与後に高頻度だったクローンはウイルス感染時に比較的低頻度になります。このことから、PNGワクチンで誘導されウイルス感染細胞を効果的に排除できるCD8陽性キラーT細胞は、普段の存在頻度は低くてもウイルス感染時には迅速に増殖できるという特徴を有すること、PNGワクチンがその誘導に優れていること、並びにワクチンの免疫活性化性能の評価において低頻度で存在するT細胞にも着目する必要があることを明らかにしました(図4)。
過去の研究から、PNGワクチンが良質なCD8陽性キラーT細胞を誘導できるのは、リンパ節内のプロフェッショナルな抗原提示細胞、特にリンパ節髄質マクロファージに選択的にワクチン抗原を送達することに依ることが分かっています(Muraoka et al., ACS Nano 2014)。しかし、なぜPNGがワクチン抗原をリンパ節髄質マクロファージに選択的に送達できるのかは長らく不明でした。今回、PNGの生理的受容体としてC型レクチンの一種であるマウスSIGN-R1(注5)を初めて同定しました。マウスSIGN-R1はリンパ節髄質マクロファージに特異的に発現しています。また、SIGN-R1ファミリーはウイルス等の表面の糖鎖を認識して細胞内に取り込む能力が高いことで知られています。以上より、PNGはSIGN-R1への結合を通じてマクロファージにワクチン抗原を効率良く送り込む働きがあると考えられます。ヒトでもDC-SIGNはリンパ節のマクロファージや樹状細胞に高発現していることから、今回の知見はヒトへの外挿性も高いと考えられます。
《社会的意義》
本研究ではPNGワクチンが、高い増殖能とウイルス排除作用を備え、長期持続性を有し、突然変異による免疫逃避の影響も少ないCD8陽性キラーT細胞の活性化を通じて、新型コロナウイルスの感染を効果的に防御できる優れたワクチン技術であることを明らかにしました。今後、新型コロナウイルス以外の病原性ウイルスに対するワクチンの開発にもPNG技術を幅広く活用できることが期待されます。
「参考資料」
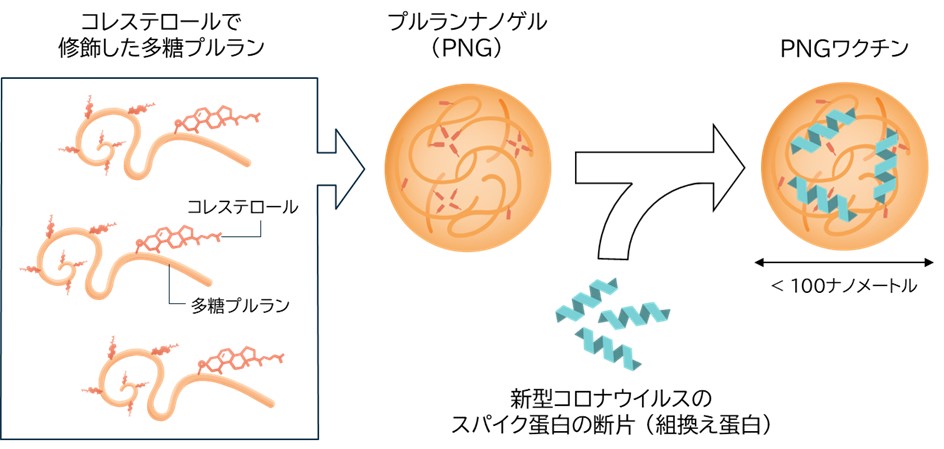 図1.PNGワクチンの構造 |
食品などの添加物として幅広く使われている多糖プルランにコレステロールを修飾したものを出発材料としてPNGを作製します。これにワクチン抗原(ここでは新型コロナウイルスのスパイク蛋白の断片)を搭載することでPNGワクチンが完成します。製造工程はシンプルでスケールアップも容易であることから、将来のパンデミックにも対応できるワクチン技術となることが期待されます。
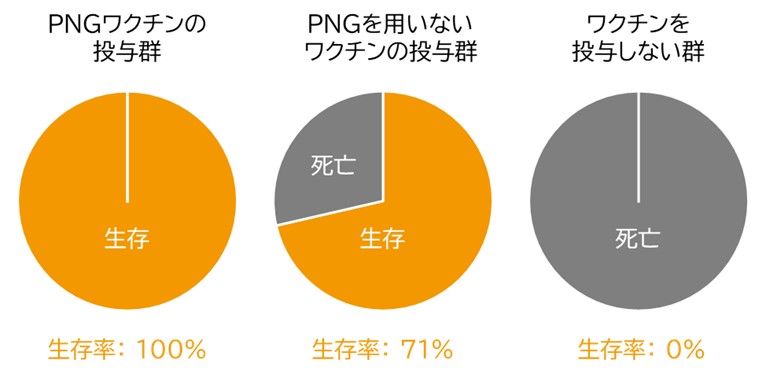 図2.PNGワクチンの新型コロナウイルスに対する感染防御効果 |
K18-hACE2マウスにPNGワクチン又はPNGを用いないワクチンを投与したのち、新型コロナウイルスの感染を行いました(n = 7)。PNGワクチン投与群は全例が生存したのに対し、PNGを用いないワクチンでは約3割のマウスが死亡しました。ワクチンを投与しない群では全例が死亡しました。
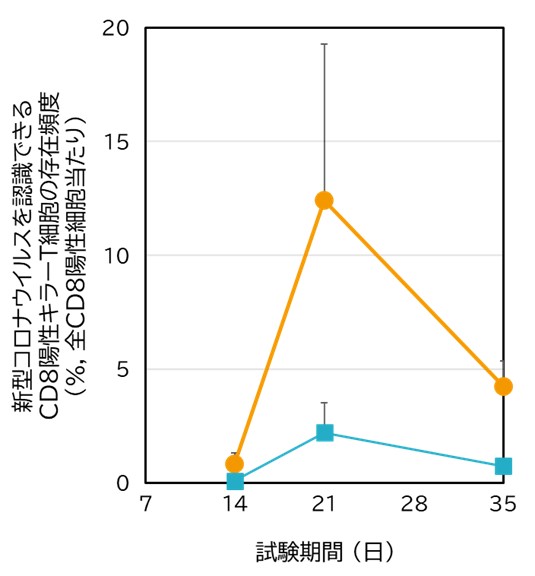 図3.PNGワクチン投与マウスにおける新型コロナウイルスに対するCD8陽性キラーT細胞の誘導 図3.PNGワクチン投与マウスにおける新型コロナウイルスに対するCD8陽性キラーT細胞の誘導 |
マウスにPNGワクチン(シンボル:●)又はPNGを用いないワクチン(シンボル:■)を投与したのち、脾臓における新型コロナウイルス認識CD8陽性キラーT細胞の存在頻度を測定しました(n = 7~10)。
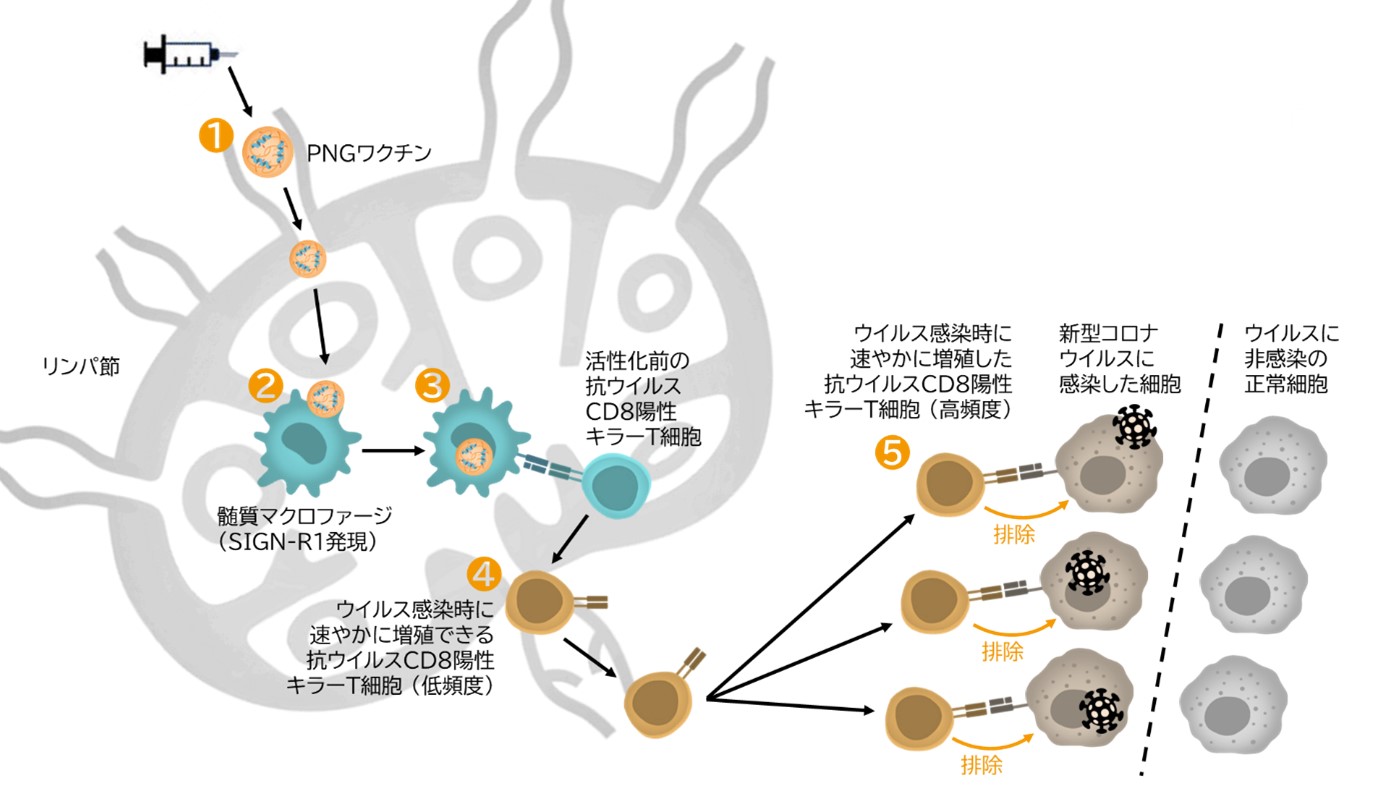 図4.PNGワクチンが優れた感染防御効果を示すメカニズム |
皮下投与されたPNGワクチンはナノ粒子であるため、速やかにリンパ節に移行します(図中❶)。リンパ節内でPNGワクチンは生理的受容体のマウスSIGN-R1(ヒトではDC-SIGN)への結合を介して髄質マクロファージに選択的に取り込まれます(❷)。髄質マクロファージはPNGワクチンに含まれるワクチン抗原をCD8陽性キラーT細胞に効率よく提示します(❸)。このときPNGワクチンは、ワクチン投与直後は低頻度でもウイルス感染時に速やかに増殖して対応できるCD8陽性キラーT細胞を誘導することができます(❹)。このCD8陽性キラーT細胞はウイルス感染時には速やかに増殖してウイルス感染細胞を効果的に排除し、感染の進行をしっかり抑止できると考えられます(❺)。CD8陽性キラーT細胞は攻撃対象の認識能力が非常に高く、ウイルスに感染していない正常細胞を攻撃することはありません。
発表者・研究者等情報
長崎大学大学院医歯薬学総合研究科 教授 池田 裕明
東京大学大学院医学系研究科 教授 MOI MENG LING(モイ メン リン)
京都大学大学院医学研究科 特任教授 秋吉 一成
愛知県がんセンター(研究所)ユニット長 村岡 大輔
ユナイテッド・イミュニティ株式会社 代表取締役会長 原田 直純
論文情報
雑誌名:npj Vaccines
題 名:Low-frequency CD8+ T cells induced by SIGN-R1+ macrophage-targeted vaccine confer SARS-CoV-2 clearance in mice
著者名:Daisuke Muraoka*, Meng Ling Moi*, Osamu Muto, Takaaki Nakatsukasa, Situo Deng, Chieko Takashima, Rui Yamaguchi, Shin-ichi Sawada, Haruka Hayakawa, Thi Thanh Ngan Nguyen, Yasunari Haseda, Takatoshi Soga, Hirokazu Matsushita, Hiroaki Ikeda, Kazunari Akiyoshi, Naozumi Harada.(*責任著者)
DOI: https://doi.org/10.1038/s41541-024-00961-6
URL: https://www.nature.com/articles/s41541-024-00961-6
研究助成
本研究は、国立研究開発法人日本医療研究開発機構(AMED) ワクチン開発のための世界トップレベル研究開発拠点の形成事業「ワクチン開発のための世界トップレベル研究開発拠点群 東京フラッグシップキャンパス(東京大学新世代感染症センター)」(UTOPIA, JP223fa627001)およびワクチン・新規モダリティ研究開発事業(243fa727001h0003)の支援により実施されました。
用語解説
(注1) プルランナノゲル(PNG):直径が100ナノメートル以下(細胞1個の約100分の1)のハイドロゲルナノ粒子。人体に無害なグルコースとコレステロールからできており、臨床試験で安全性が高いことが確認されている。
(注2) マクロファージ:白血球の1種。貪食細胞で、死んだ細胞や侵入したウイルス・細菌などの異物を捕食して消化し排除する。優秀な抗原提示細胞でもあり、感染やがん等の病態における免疫機能の中心的役割を担う。
(注3) CD8陽性キラーT細胞:細胞の表面に CD8 と呼ばれるマーカー蛋白を有し、病原体感染細胞やがん細胞に対する傷害機能を発揮するT 細胞。
(注4) T細胞受容体(TCR):T細胞の細胞膜上に発現する抗原認識受容体蛋白。
(注5) SIGN-R1(CD209b):主にマウスのリンパ節髄質マクロファージや脾臓の辺縁帯マクロファージが発現するC型レクチン(糖鎖受容体)。






 受験生
受験生 在学生
在学生 卒業生
卒業生 保護者等
保護者等 地域・一般
地域・一般 企業・研究者
企業・研究者 教職員
教職員